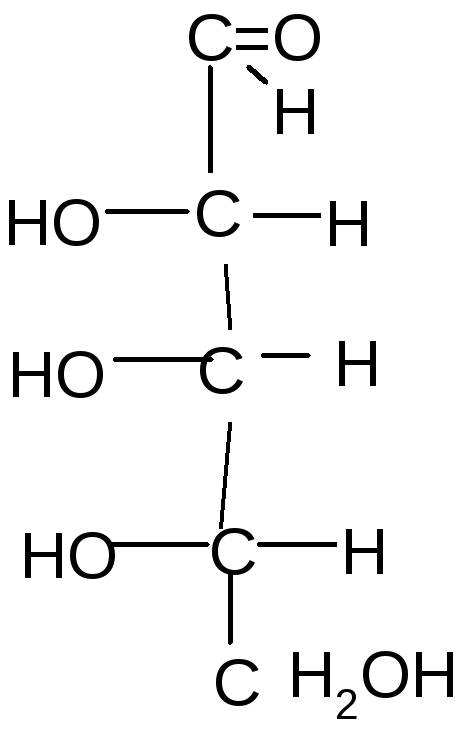
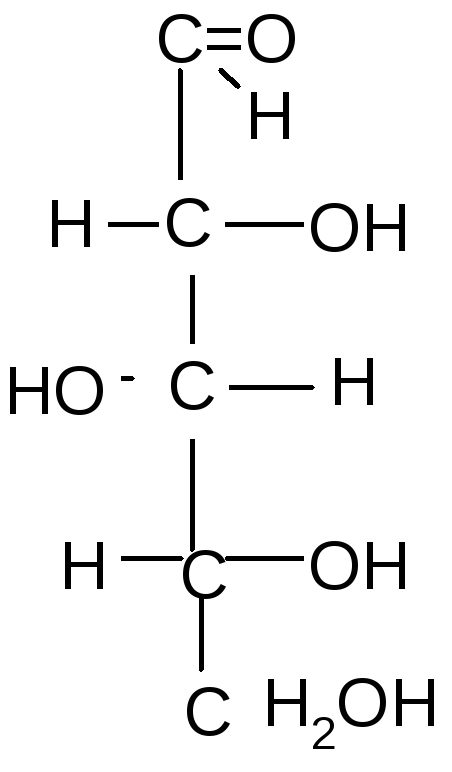
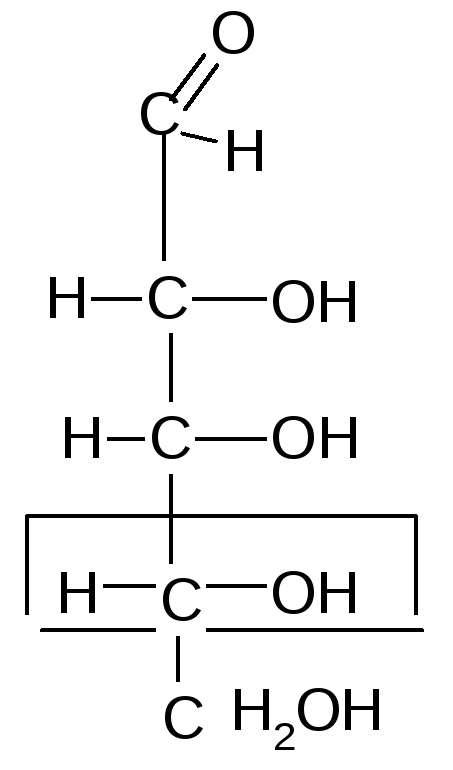
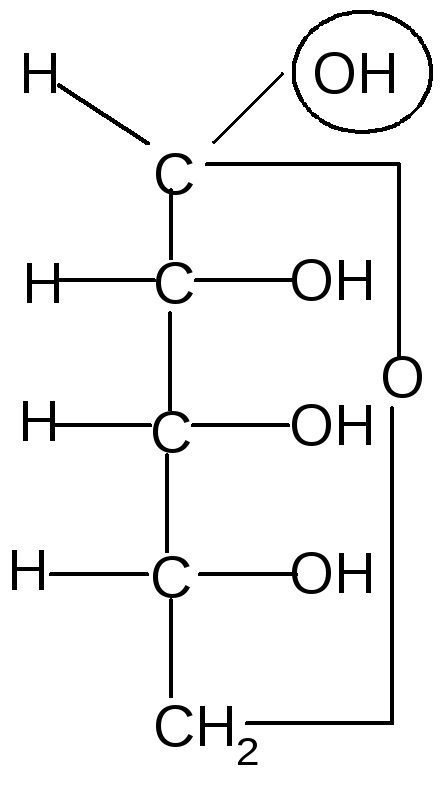
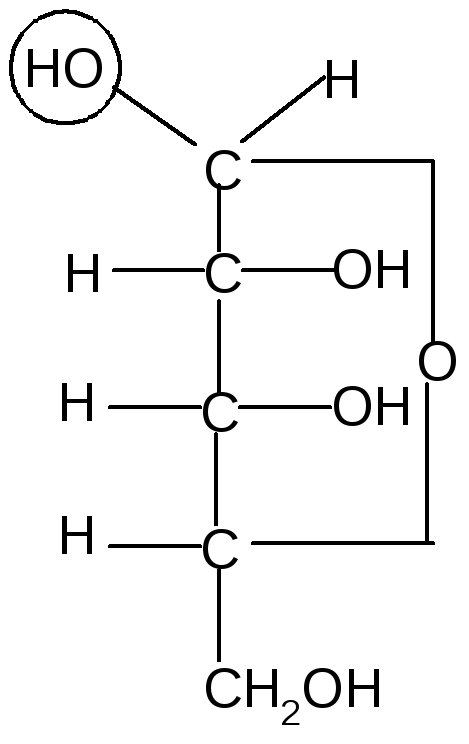
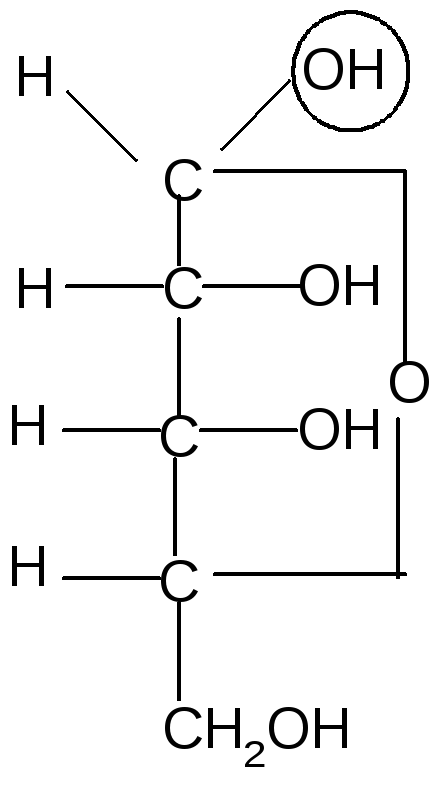
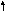31.Изомерия моносахаридов: стереоизомерия, цикло-оксо-таутомерия, а- и в-аномерия на примере глюкозы.
32.Строение наиболее важных представителей пентоз (рибоза, ксилоза, рибулоза), гексоз (глюкоза, галактоза, манноза, фруктоза), дезоксисахаров (2-дезоксирибоза), 2-амигносахаров (глюкозамин, маннозамин, галактозамин).
Пентозы — химическое название класса пятиуглеродных моносахаридов, то есть сахаров, общей формулой которых является C5(H2O)5, или C5H10O5.
Рибоза, ксилоза, рибулоза
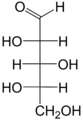

Гексозы, C6H12O6, простые сахара — моносахариды.
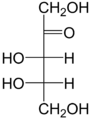
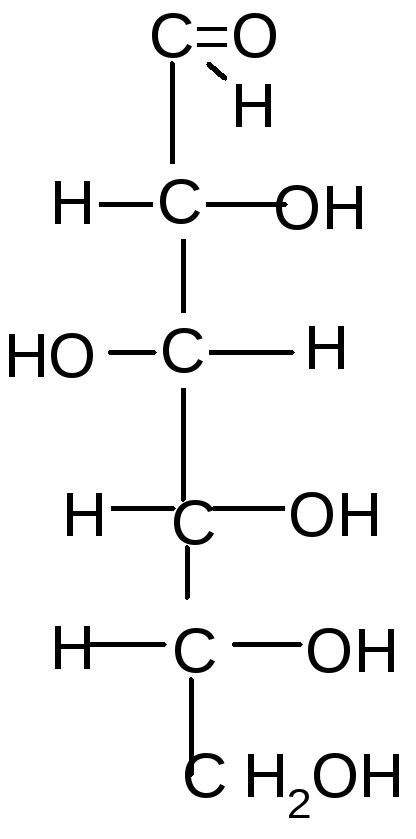
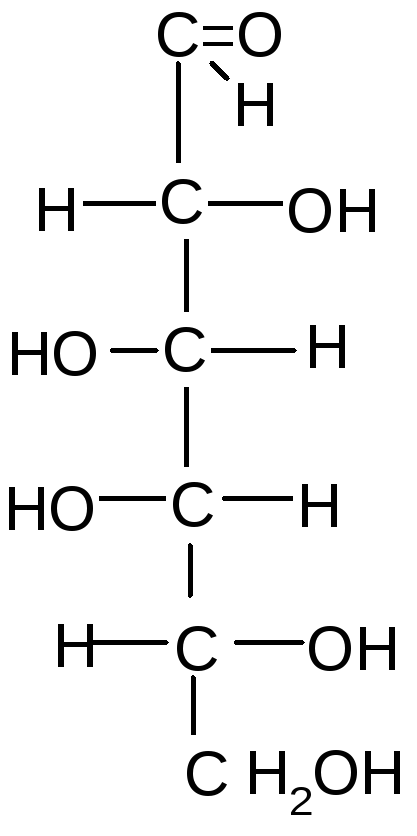
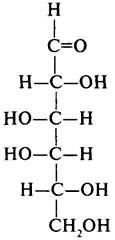
Глюкоза, галактоза, манноза, фруктоза
, 
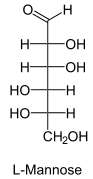
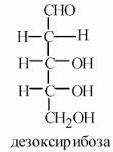
Дезоксисахара (2-дезоксирибоза)
глюкозамин, галактозамин, маннозамин
ЗЗ.Химические свойства моносахаридов: окисление моносахаридов (образование оновых, аровых, уроновых кислот); восстановление моносахаридов (образование ксилита, сорбита, маннита); реакции этерификации по спиртовой группе с образованием фосфорных эфиров; реакции изомеризации: превращение глю-6-фосфата во фруктозу-6-фосфат, глюкозу-1-фосфат, рибулозы-5-фосфата в ксилулозу-5-фосфат; образование О- N— гликозидов, условия их гидролиза.
Химические свойства глюкозы
1. Реакция серебряного зеркала: Качественная реакция
СH2OH(CHOH)4-COH + Ag2O t . NH 3 → СH2OH(CHOH)4-COOH + 2Ag↓(глюконовая кислота)
2. Окисление гидроксидом меди (II):
III. Свойства многоатомных спиртов
1. Образование простых эфиров со спиртами
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу.
Источник
Тема 8-1. Углеводы. Моносахариды Теория
Углеводы широко распространены в природе. В организме животных на углеводы приходится до 2 %, а в растениях – до 90 % сухого вещества. Эти вещества выполняют энергетическую, структурную, защитную и другие функции; входят в состав нуклеиновых кислот, коферментов и витаминов; используются в качестве лекарственных препаратов.
В зависимости от строения углеводы классифицируют на моно-, олиго- и полисахариды.
Моносахариды (монозы)– это многоатомные альдегидо- и кетоноспирты, не гидролизующиеся до более простых.
По числу атомов углерода моносахариды подразделяют на тетрозы (С4 ),пентозы (С5),гексозы (С6)и т.д.
Моносахариды, содержащие альдегидную группу, называют альдозами; кетонную –кетозами.
Важнейшие природные моносахариды Альдопентозы
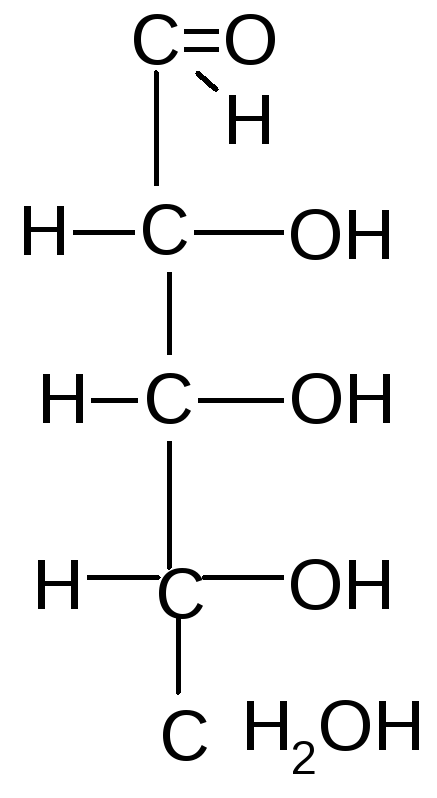
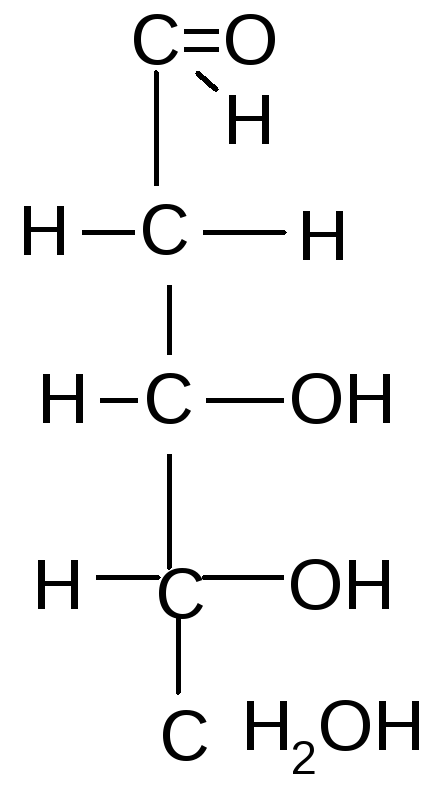
Альдогексозы Кетогексоза

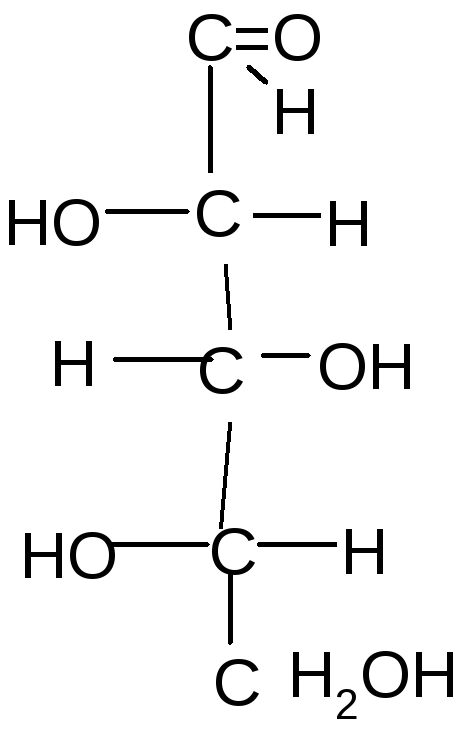
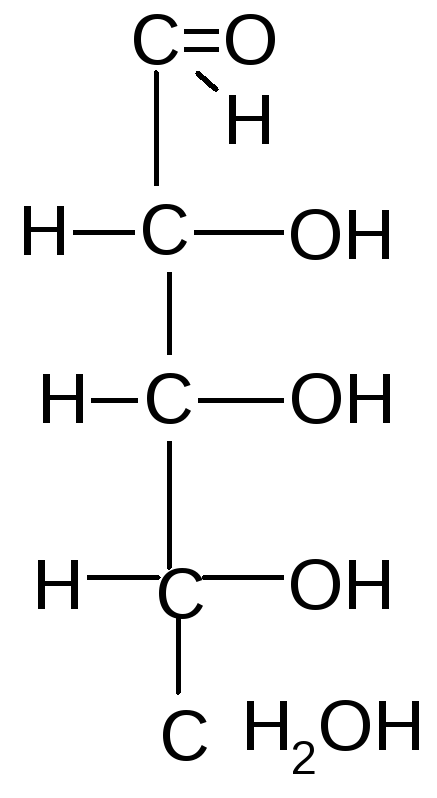

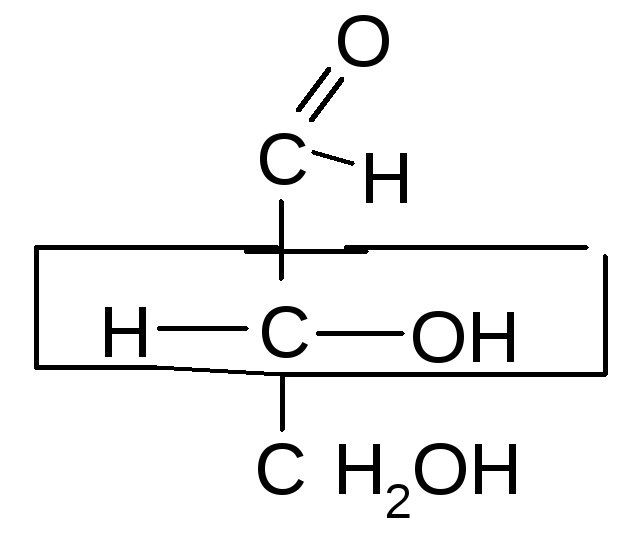
- Цикло-цепные таутомеры моносахаридов
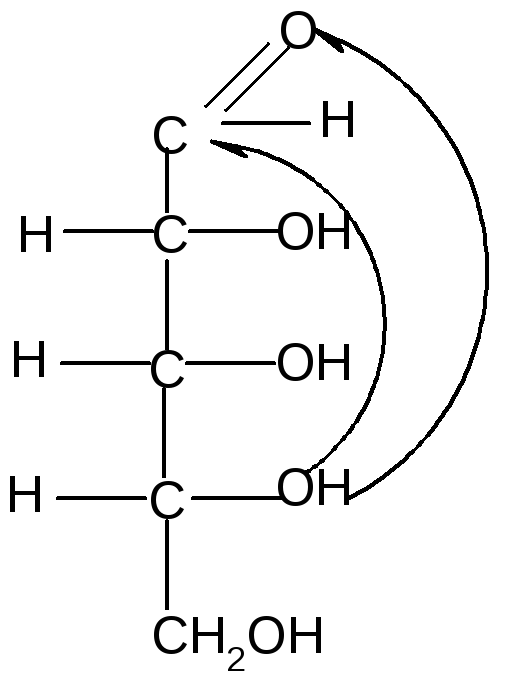
По мере изучения свойств моносахаридов выяснилось, что открытые (цепные) формулы не описывают полностью химическое поведение сахаров. Например, несмотря на наличие в молекуле глюкозы пяти ОН– групп, только одна из них вступает в реакцию со спиртами в присутствии сухого хлористого водорода с образованием гликозидов. Для объяснения подобных противоречий было высказано предположение (1870 г. А. Колли; 1883 г. Б. Толленс), что истинное строение моноз не описывается лишь открытой (цепной) формулой. Моносахариды образуют в водном растворе таутомерные смеси открытых и циклических форм. В основе их образования лежит внутримолекулярная реакция нуклеофильного присоединения спиртовых групп к альдегидной или кетонной группе: 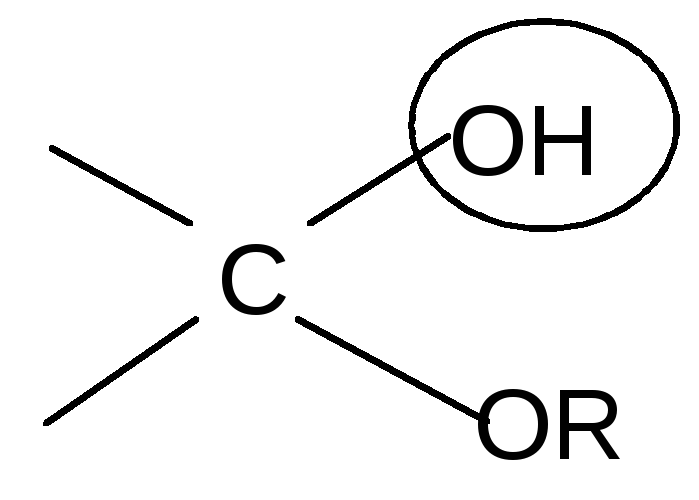
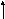



Источник