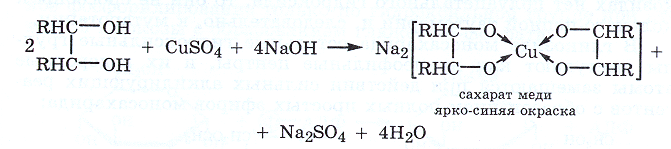- Лабораторная работа №4 Качественные реакции на углеводы
- Реакция Троммера
- Реакция Фелинга
- Реакция серебряного зеркала по Толленсу
- Глюкоза, 1% раствор.
- Фруктоза, 1% раствор.
- Реакция Мура-Геллера
- Глюкоза, 1% раствор.
- Фруктоза, 1% раствор.
- Реакция с метиленовой синькой
- Глюкоза, 1% раствор.
- Фруктоза, 1% раствор.
- Гидроксид натрия, 10% раствор.
- Реакция Селиванова на кетогексозы
- I. Доказательство наличия -он групп
- II. Реакции с участием карбонильной группы-
- III. Реакция Селиванова на фруктозу
Лабораторная работа №4 Качественные реакции на углеводы
Многие качественные реакции углеводов основаны на восстанавливающих свойствах свободных карбонильных групп (свободного гликозидного гидроксила) сахаров. Эти же реакции применяются для большинства количественных методов определения углеводов.
Моносахариды обладают свойствами как спиртов, так и карбонильных соединений. При восстановлении карбонильной группы металлами (серебро, медь, висмут, железо и др.) в щелочной среде образуются многоатомные спирты. При окислении в первую очередь окисляется карбонильная группа, превращаясь в карбоксильную, а затем возможно окисление спиртовых гидроксилов. Металлы при этих реакциях восстанавливаются из окисной формы в закисную или даже до свободного состояния. На способности моносахаридов восстанавливать различные соединения основаны методы качественного и количественного определения моносахаридов.
Фруктоза также дает реакции восстановления металлов, хотя она имеет не альдегидную, а кетонную группу, которой не свойственно окисляться слабыми окислителями. Это объясняется тем, что в щелочной среде фруктоза легко превращается в глюкозу, которая и проявляет восстанавливающие свойства.
Определение содержания глюкозы в крови и обнаружение ее в моче играет важную роль в клиническом исследовании.
Дисахариды, имеющие свободный глюкозидный гидроксил (мальтоза, лактоза, целлобиоза), дают реакции восстановления металлов. Дисахариды сахароза и трегалоза, не имеющие свободного глюкозидного гидроксила, не дают этих реакций.
Реакция Троммера
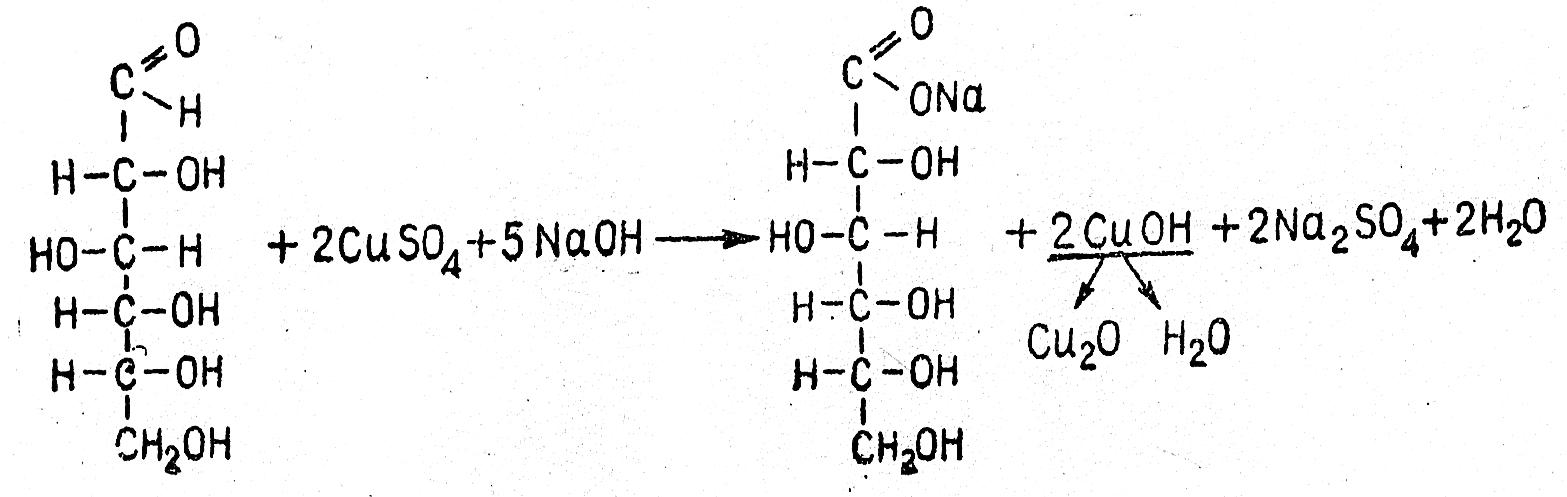
Реакция обусловлена окислением моносахарида и восстановлением гидрата окиси меди в гидрат закиси или закись меди. Схематично реакция может быть изображена следующим образом:
- Глюкоза, 1% раствор.
- Фруктоза, 1% раствор.
- Сахароза, 1% раствор.
- Мальтоза, 1% раствор.
- Гидроксид натрия, 10% раствор.
- Сульфат меди, 5% раствор.
Реакция Фелинга
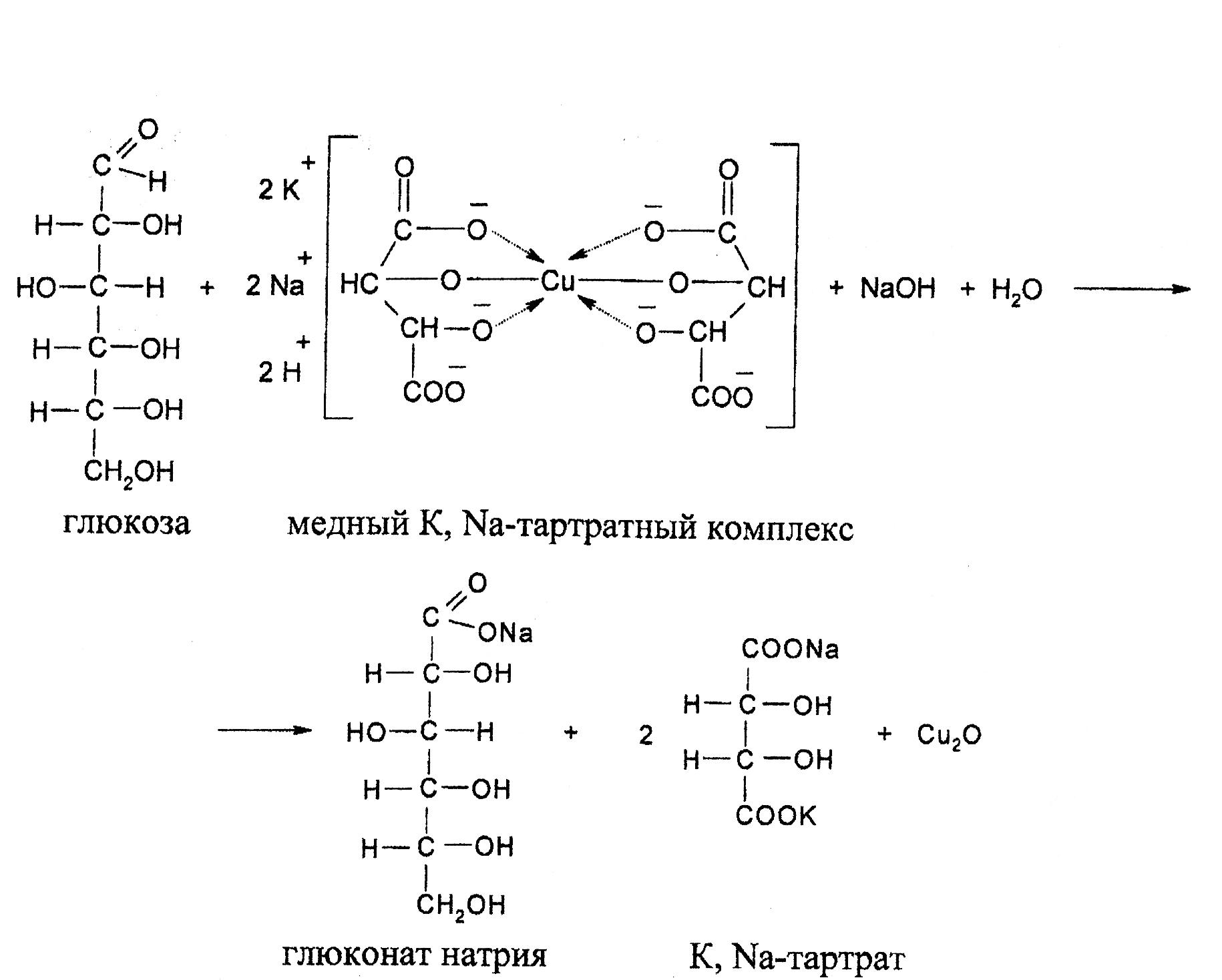
Реакция Фелинга является модификацией реакции Троммера, в которой вместо Cu(OH)2 применяется алкоголят меди с сегнетовой солью (K, Na-виннокислый) в щелочной среде. Химизм реакции тот же, что и в реакции Троммера. Преимуществом фелинговой жидкости является то, что медь при избытке реактива не выпадает в осадок в виде оксида меди (II). Раствор Фелинг I представляет собой приблизительно 7% водный раствор СuSO4. 5H2O. Раствор Фелинг II представляет собой раствор сегнетовой соли в едкой щелочи. При сливании растворов I и II образуется растворимая медная комплексная соль типа алкоголята меди синего цвета. Алкоголяты меди при нагревании разрушаются в присутствии моносахаридов с образованием алкоголятов сахара с последующим их разрушением. Реактивы:
- Глюкоза, 1% раствор.
- Фруктоза, 1% раствор.
- Сахароза, 1% раствор.
- Мальтоза, 1% раствор.
- Раствор Фелинга.
Проведение опыта В пробирку наливают 1 мл раствора глюкозы и добавляют равный объем реактива Фелинга. Смесь нагревают на спиртовке до кипения. Образовавшийся красный осадок оксида меди (I) свидетельствует о положительной реакции на реактив Фелинга. Проделать реакцию Фелинга с фруктозой, сахарозой, мальтозой.
Источник
Реакция серебряного зеркала по Толленсу
Заключается в восстановлении моносахаридами аммиачного раствора окиси серебра до металлического серебра.
Глюкоза, 1% раствор.
Фруктоза, 1% раствор.
Реакция Мура-Геллера
Глюкоза, 1% раствор.
Фруктоза, 1% раствор.
Реакция с метиленовой синькой
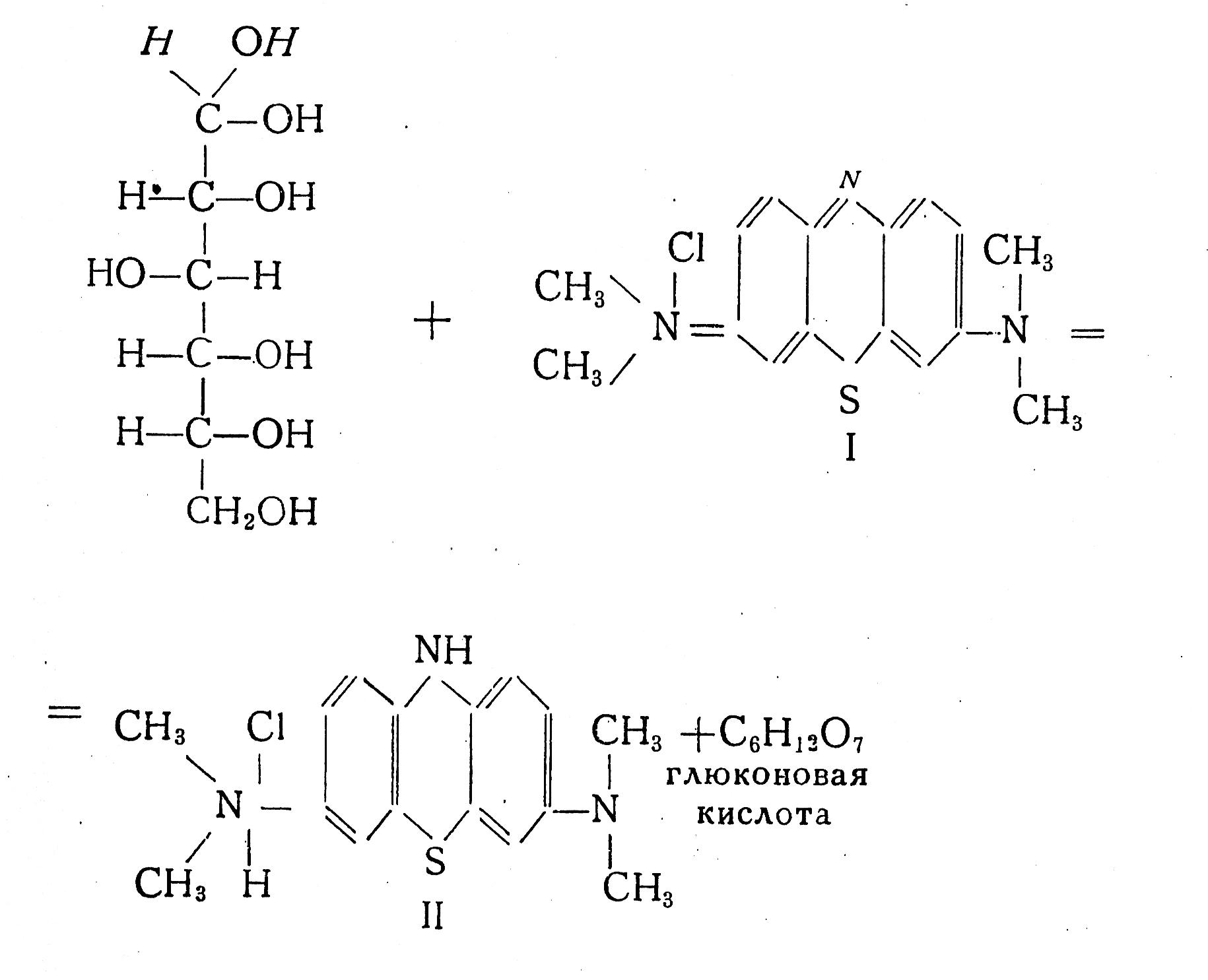
В щелочной среде метиленовая синька окисляет (путем дегидрирования) гидратную форму моносахарида до монокарбоновой кислоты. При этом метиленовая синька (синего цвета I) восстанавливается до лейкометиленовой сини (бесцветное соединение II). Гидратная форма сахаров обычно образуется в водной среде при наличии альдегидной формы сахара. При этом альдегидная форма сахара присоединяет к себе молекулу воды. Химизм реакции: Реактивы:
Глюкоза, 1% раствор.
Фруктоза, 1% раствор.
Гидроксид натрия, 10% раствор.
Реакция Селиванова на кетогексозы
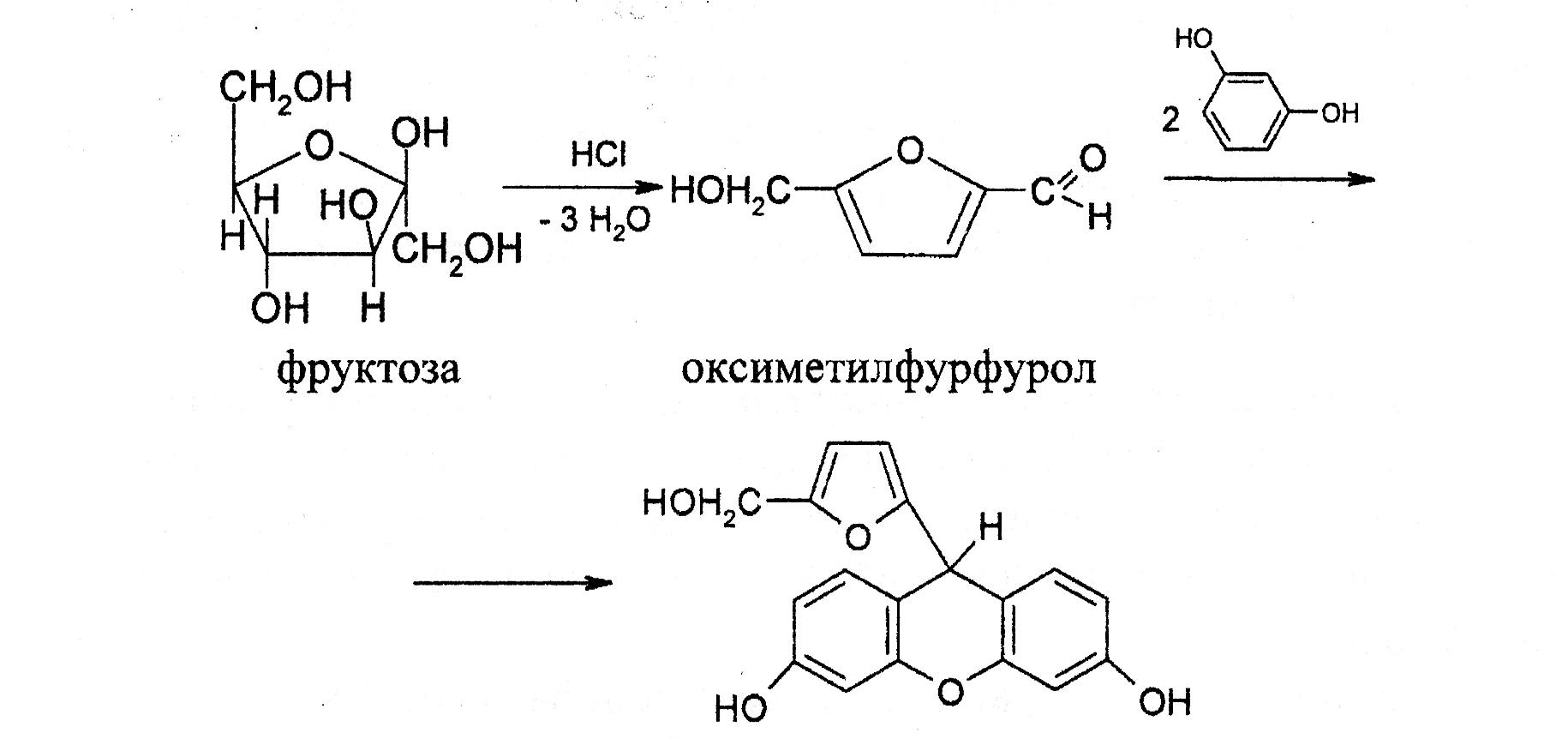
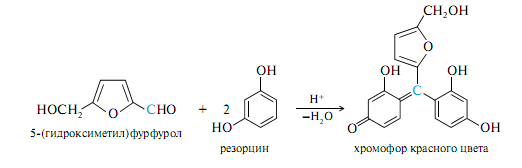
При нагревании фруктозы (и других гексоз) с соляной кислотой образуется оксиметилфурфурол, который с резорцином образует соединение, окрашенное в вишнево-красный цвет. Альдозы также дают эту реакцию, но реакция у них протекает медленнее и в особых условиях (температура и кислотность среды), поэтому реакция Селиванова применяется для открытия кетоз. Реактивы:
Источник
I. Доказательство наличия -он групп
Моносахариды, подобно глицерину, в водных растворах взаимодействуют со свежеобразованным гидроксидом меди с образованием сахаратов ярко-синего цвета, которые устойчивы, так как являются хелатными комплексами катиона меди.
II. Реакции с участием карбонильной группы-
а)Альдозы. Реакции мягкого окисления углеродного атома альдегидной группы катионами 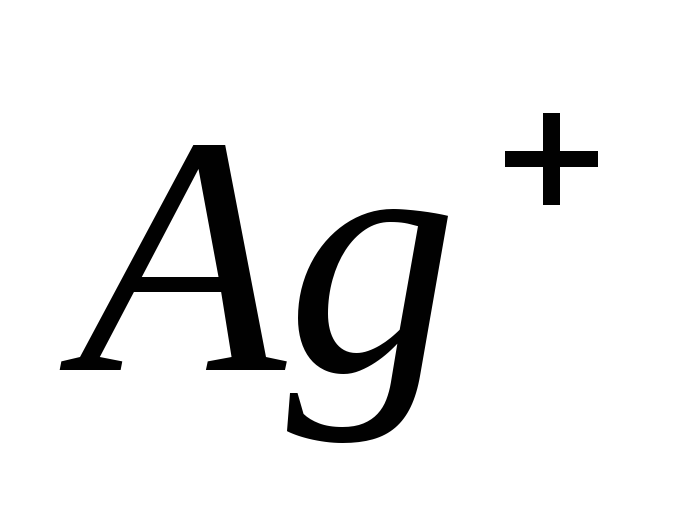




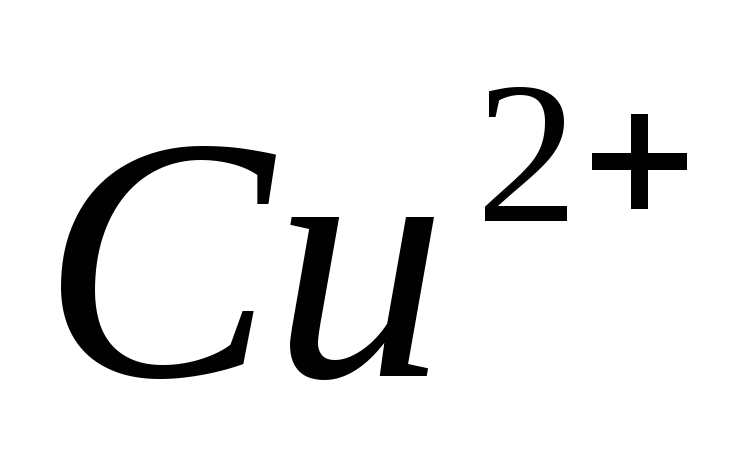
Блестящий налет на стенках пробирки
Продукты окисления альдегидной группы альдоз называются гликоновыми кислотами.
Гликозиды не дают положительной пробы с этими реагентами, так как не могут самопроизвольно образовать альдозу.
б) Кетозы. Несмотря на устойчивость кетонов к окислению, также дают положительные пробы Фелинга и Толленса. Объясняется это тем, что в щелочной среде, в которой проводятся эти реакции, кетозы частично изомеризуются в альдозы.
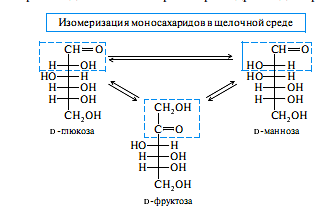
Изомеризация (кето-енольная таутомерия):
Первой стадией изомеризации альдоз является обратимое образование 1,2-ендиоль-ной структуры под действием основания при участии СН-кислотного центра — атома С-2. Превращение ендиола в карбонильную форму происходит тремя путями (а — в), как показано на схеме. Путь а приводит к кетозе; два других пути отличаются стерической напраатенностью, в результате чего образуются исходная альдоза (путь б) и ее эпимер по С-2 (путь в).
Например, D-глюкоза в растворе гидроксида кальция за 20 дней при 20 °С образует 29% D-фруктозы и 1 % D-маннозы, а с D-маннозой за сутки в 0,5 М растворе гидроксида натрия превращение происходит на 28% и в растворе гидроксида бария — на 40%.
1) . Как и в щелочной среде, начинаются с енолизации фрагмента С-1—С-2.
2) Дальнейшие превращения 1,2-ендиола связаны не только с образованием изомерных карбонильных соединений или разрывом связи С—С, но и с отщеплением молекулы воды. Одно из направлений дегидратации сопровождается образованием производных фурфурола, которое приводится ниже только схематически. Из пентоз при этом получается фурфурол, из гексоз — 5-(гидроксиметил) фурфурол.
Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов, в частности глюкозы в биологических жидкостях (моча, кровь).
III. Реакция Селиванова на фруктозу
Для кетоз характерна реакция Селиванова- нагревание с хлороводородной кислотой в присутствии резорцина, приводящее к продуктам, окрашенным в красный цвет, альдозы дают более слабую окраску только при длительном нагревании.
В реакцию Селиванова кетозы (фруктоза) вступает легче гексоз и на этом основано определение фруктозы в присутствии других сахаров.
Пентозы с НCl и флороглюцином дают фиолетово-красную окраску раствора.
Источник