Количественное определение листьев брусники
Представлены результаты разработки методикиколичественного определения арбутина в брусники листьях (Vitis – idaeaefolia) и толокнянки листьях (Uvaeursifolia) методом капиллярного электрофореза. Показано, что использование боратного электролита с рН 9,0 является достаточным для ионизации арбутина. При этом рабочие параметры были следующие: кварцевый капилляр диаметром 50 мкм с эффективной длинной 65 см; детектирование осуществлялось спектрофотометрически при 254 нм; напряжение составляло 20 кВ. В указанных условиях удалось достигнуть приемлемого разделения арбутина с сопутствующими компонентами сырья. Разработанная методика была подвергнута процедуре валидации по показателям: линейность, прецизионность и правильность. С использование разработанной и валидированной методики установлено следующее содержание арбутина в сырье: брусники листья (ОАО «Красногорсклексредства», серия 80614) – 6,21%±0,27, толокнянки листья (ОАО«Красногорсклексредства», серия 80714) – 14,49%±0,54.
1. Толокнянка обыкновенная Arctostaphylosuva-ursi (L.) Spreng. Р. В. Куцик, Б. М. Зузук., А.Т. Недоступ, Т. Пецко. Провизор Выпуск №18 2003 (http://www.provisor.com.ua/archive/2003/N18/art_27.php).
2. Моисеев Д.В. Кинетика реакции деструкции арбутина в листьях брусники обыкновенной при хранении в естественных и стрессовых условиях // Курский научно-практический вестник «Человек и его здоровье».2013. №2. С. 106-111.
3. Thongchai W, Liawruangrath B, Liawruangrath S. High-performance liquid chromatographic determination of arbutin in skin-whitening creams and medicinal plant extracts.// J Cosmet Sci.2007. Jan-Feb;58(1). P. 35-44.
4. Руководство по методам контроля качества и безопасности биологически активных добавок к пище.—М.: Федеральный центр госсанэпиднадзора Минздрава России, 2004.—240 с.
5. Guidelines for standard method performance requirements. − [Электронный ресурс]. − Режим доступа:http://www.aoac.org/imis15_prod/AOAC_Docs/StandardsDevelopment/eoma_appendix_f.pdf.
На сегодняшний день неотъемлемой частью номенклатуры лекарственных средств назначаемых в комплексной терапии воспалительных заболеваний мочевого пузыря и мочевыводящих путей (циститы, уретриты) является лекарственное растительное сырье, основные из которых это брусники листья (Vitis – idaeae folia) и толокнянки листья (Uvae ursi folia). Мочегонные и уроантисептические свойства данных растительных объектов связаны в первую очередь с фенольными гликозидами арбутином и метиларбутином, а также с гидрохиноном и его метиловым эфиром [1].
Согласно нормативной документации на данные виды сырья, содержание арбутина в них должно быть не менее 6 % (толокнянки листья) и 4,5 % (брусники листья).
Следует сказать, что все нормативные документы на указанные виды сырья в качестве методики количественного определения арбутина предлагают использовать окислительно-восстановительное титрование йодом. Важно также отметить, что методика обременена сложными процедурами пробоподготовки и очистки, занимающими длительное время и невольно приводящими к возрастанию случайной погрешности. Кроме того, в итоге осуществляется титрование не только арбутина, а некоего комплекса, близких по химическим свойствам, веществ, что также не позволяет оценить истинное содержание арбутина.
Решение указанных вопросов возможно с использованием сепарационных методов анализа (ВЭЖХ, капиллярного электрофореза (КЭ)). И на сегодняшний день известно ряд ВЭЖХ-методик количественного определения арбутина в сырье 3. В то же время использование КЭ может быть более оправданным, поскольку не требуется дорогостоящих растворителей и колонок. Кроме того, наличие более высоких параметров эффективности является ключевым преимуществом при анализе сложных растительных объектов, содержащих десятки, а порой и сотни соединений.
Цель работы
Разработка и валидация методики количественного определения арбутина в толокнянки листьях и брусники листьях с применением капиллярного электрофореза.
Материалы и методы исследования
Для исследования использовали стандартный образец (СО) арбутина (Sigma, с содержанием не менее 98%), а так же образцы сырья толокнянки листья (ОАО «Красногорсклексредства», серия 80714) и брусники листья (ОАО «Красногорсклексредства», серия 80614).
Работу проводили с использованием системы капиллярного электрофореза Капель 103 Р (группа компаний Люмэкс, Россия) с кварцевым капилляром диаметром 50 мкм, общей длинной 75 см и эффективной длинной 65 см. Детектирование осуществляли спектрофотометрически при 254 нм в катодной области капилляра. Напряжение составляло 20 кВ (блок положительной полярности). Для подготовки капилляра и восстановления его поверхности проводили его последовательную промывку водой, 0,5 М раствором кислоты хлористоводородной, водой, 0,5 М раствором натрия гидроксида, водой и затем ведущим электролитом.
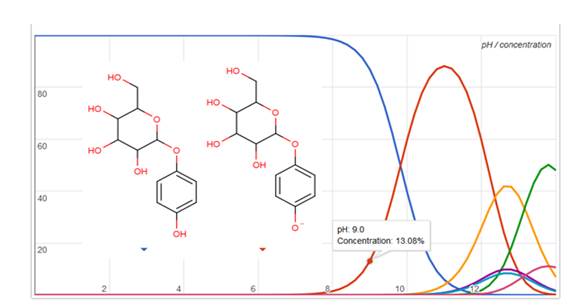
В работе реализовывался вариант зонного электрофореза, где в качестве ведущего электролита использовали 0,01М боратный буферный раствор с рН 9,0. Выбор электролита связан с тем, что при данном значении рН, арбутин ионизируется по фенольному гидроксилу (Рисунок 1), являясь при этом заряженной частицей.
Рисунок 1. Зависимость степени ионизации арбутина от рН среды (по данным http://www.chemicalize.org).
Важно отметить, что при данном значении рН электролита арбутин ионизирован всего на 13 %, однако даже в этих условиях он обладает, хоть и незначительной, эффективной электрофоретической подвижностью.
Извлечение арбутина из сырья проводили в соответствии с методикой, приведенной в нормативной документации на анализируемое лекарственное растительное сырье. Для этого точную навеску (около 0,5 г) сырья помещали в коническую колбу вместимостью 100мл, заливали 50 мл воды и присоединяли к обратному холодильнику. Нагревание вели на плитке, поддерживая слабое кипение, в течение 30 минут. Горячее извлечение фильтровали в мерную колбу вместимостью 100 мл через бумажный фильтр диаметром 7 см. В колбу с сырьем повторно прибавляли 25 мл воды и кипятили в течение 20 минут. Повторное горячее извлечение фильтровали, объединяя извлечения. Остаток на фильтре промывали 20 мл горячей воды, также объединяя все извлечения. После охлаждения раствор доводили до метки водой и перемешивали. Далее 1 мл полученного раствора центрифугировали 5 мин при 8000 мин-1 и подвергали его анализу.
Результаты исследования и их обсуждение
На рисунках 2-4 представлены электрофореграммы раствора СО арбутина, а также извлечений брусники листьев и толокнянки листьев.
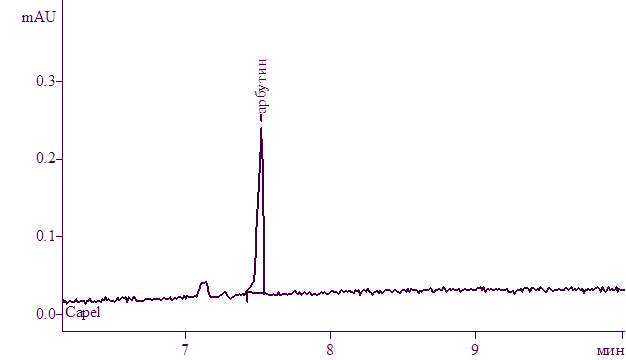
Рисунок 2. Электрофореграмма раствора СО арбутина
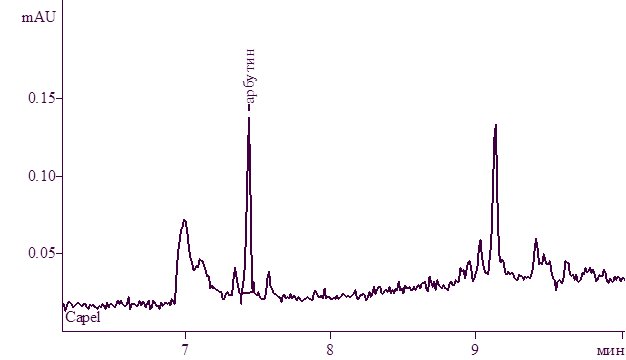
Рисунок 3. Электрофореграмма извлечения брусники листьев
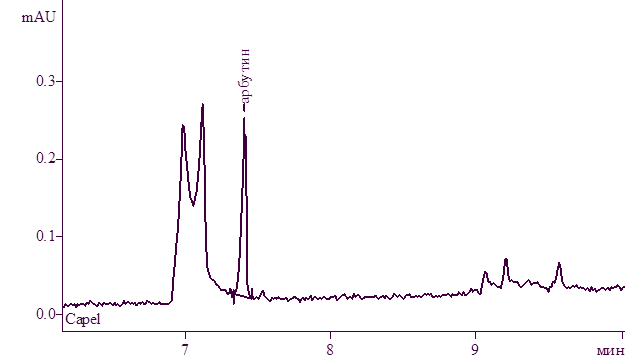
Рисунок 4. Электрофореграмма извлечения толокнянки листьев
В результате в обоих видах сырья было установлено наличие арбутина. При этом коэффициент его разделения с сопутствующими компонентами пробы был достаточным для его количественного определения.
Следующим этапом исследований была валидационная оценка разработанной методики по показателям: линейность, прецизионность и правильность.
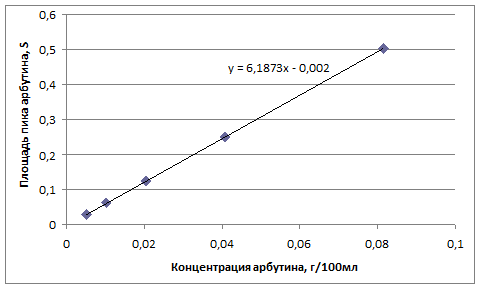
Линейность методики определялась по итогам анализа серии растворов СО арбутина различной концентрации (от 0,0051 до 0,0816 г/100мл). На рисунке 5 представлен градуировочный график зависимости площади пика арбутина от его концентрации в растворе. Полученная зависимость имеет линейный характер и описывается следующим уравнением: y=6,1873x-0,002. При этом коэффициент корреляции (r) был равен 0,999995, что позволяет использовать данное уравнение для количественного определения арбутина в указанном диапазоне концентраций.
Рисунок 5. Градуировочный график зависимости площади пика от концентрации арбутина в растворе
Для установления прецизионности (воспроизводимости) проводили 6 параллельных определений для каждого образца сырья. Расчет содержания (%) проводили по уравнению градуировочного графика арбутина, в пересчете на воздушно сухое сырье. Результаты оценки прецизионности методики количественного определения арбутина в брусники листьях и толокнянки листьях приведены в таблице 1-2.
Результаты оценки прецизионности методики количественного определения арбутина в брусники листьях
Источник
FOLIA VACCINII VITIS-IDAEA
Собранные до начала цветения или после созревания плодов и высушенные листья многолетнего вечнозеленого дикорастущего кустарничка брусники обыкновенной — Vaccinium vitis-idaea L., сем. вересковых — Ericaceae.
Внешние признаки. Цельное сырье. Листья короткочерешковые, кожистые, эллиптические или обратнояйцевидные, на верхушке притупленные или слабовыемчатые с цельными или слегка зазубренными, завернутыми вниз краями, длиной 7-30 мм, шириной 5-15 мм. Листья сверху темно-зеленые, снизу светло-зеленые с ясно заметными темно-коричневыми точками (железками). Запах отсутствует. Вкус горький, вяжущий.
Измельченное сырье. Кусочки листьев различной формы, проходящие сквозь сито с отверстиями диаметром 3 мм. Цвет от светло-зеленого до темно-зеленого. Запах отсутствует. Вкус горький, вяжущий.
Микроскопия. При рассмотрении листа с поверхности видны слегка извилистые стенки клеток верхнего и нижнего эпидермиса. Устьица мелкие, окружены двумя околоустьичными клетками, расположенными параллельно устьичной щели (парацитный тип). На нижней стороне листа имеются железки. Они состоят из многоклеточной ножки, постепенно переходящей в овальную многоклеточную головку с коричневым содержимым. По жилкам встречаются редкие одноклеточные прямые или изогнутые волоски с толстыми стенками и гладкой или слабобородавчатой поверхностью. В мезофилле содержатся редкие одиночные призматические кристаллы оксалата кальция.
Качественные реакции. Измельченные листья в количестве 0,5 г (см. раздел «Количественное определение») кипятят с 10 мл воды в течение 2-3 мин и фильтруют через бумажный фильтр.
К 1 мл фильтрата (в фарфоровой чашке) прибавляют 4 мл раствора аммиака и по каплям 1 мл 10% раствора натрия фосфорно-молибденовокислого в хлористоводородной кислоте; появляется синее окрашивание (арбутин).
К 2-3 мл фильтрата (в фарфоровой чашке) прибавляют 2-3 капли раствора железоаммониевых квасцов; появляется зеленовато-черное окрашивание (дубильные вещества).
Примечание. Приготовление 10% раствора натрия фосфорно-молибденовокислого: 10 г натрия фосфорно-молибденовокислого растворяют в 75,6 мл концентрированной хлористоводородной кислоты.
Числовые показатели. Цельное сырье. Арбутина не менее 4,5%; влажность не более 13%; золы общей не более 7%; золы, нерастворимой в 10% растворе хлористоводородной кислоты, не более 0,5%; листьев почерневших и побуревших с обеих сторон не более 7%; измельченных частиц, проходящих сквозь сито с отверстиями диаметром 3 мм, не более 2%; других частей растения не более 1%; органической примеси не более 1%; минеральной примеси не более 0,5%.
Измельченное сырье. Арбутина не менее 4,5%; влажность не более 13%; золы общей не более 7%; золы, нерастворимой в 10% растворе хлористоводородной кислоты, не более 0,5%; кусочков почерневших и побуревших листьев не более 7%; частиц, не проходящих сквозь сито с отверстиями диаметром 3 мм, не более 5%; органической примеси не более 1%; минеральной примеси не более 0,5%.
Количественное определение см. статью «Folia Uvae Ursi».
Упаковка. Цельное сырье упаковывают в мешки тканевые или льно-джуто-кенафные не более 25 кг нетто. Измельченное сырье фасуют по 100 г в пакеты бумажные типа II с последующим вложением в пачки картонные 8-1-4.
Срок годности 3 года.
При использовании материалов сайта указывайте пожалуйста ссылку на первоисточник: https://herbarius.info/pharmacopaea/folia_vitis-idaea/
Источник
Задача 7. 6. На фармацевтическое предприятие поступило сырье «Листья брусники» для получения мочегонного сбора
6. На фармацевтическое предприятие поступило сырье «Листья брусники» для получения мочегонного сбора. Требуется стандартизировать сырье по содержанию действующих веществ.
• Укажите химический состав и формулу основного действующего вещества.
• Представьте схемы методик качественного и количественного определения действующих веществ в листьях брусники с теоретическим обоснованием.
Листья брусники содержат арбутин (4 — 9%), гидрохинон; галловую, эллаговую, хинную и урсоловую кислоты; флавоноиды, дубильные вещества.
1. К 1 мл фильтрата прибавляют раствор аммиака и раствор натрия фосфорно-молибденово-кислого в хлористоводородной кислоте; появляется синее окрашивание (арбутин).
2. К фильтрату прибавляют раствор железоаммониевых квасцов; появляется зеленовато-черное окрашивание (дубильные вещества).
Аналитическую пробу измельченного сырья экстрагируют водой. → К фильтрату прибавляют раствора свинца ацетата основного → образуется осадок. → Жидкость полностью отфильтровывают. → к фильтрату прибавляют концентрированной серной кислоты. → Прибавляют цинковой пыли. → затем жидкость нейтрализуют по лакмусовой бумаге натрия гидрокарбонатом. → Титруют раствором йода до появления синего окрашивания, не исчезающего в течение 1 мин (индикатор – крахмал) → Содержание арбутина в пересчете на абсолютно сухое сырье в процентах вычисляют по формуле.
Источник